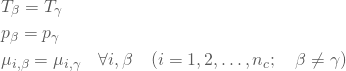実は、複数の相が共存して平衡状態を形成しているとき、あらゆる示強性変数が系のどこでも一致することは簡単に示せる。液相と気相が共存している様子を思い浮かべてほしい。系全体としてみると、そのような二相共存の系は不均質である。しかし、液相だけ切り取ったり、気相だけ切り取ったりすると、どちらも均質な平衡状態であることが分かる。液相と気相の間には仕切りや壁の類の拘束条件は存在しないので、平衡状態における示強性変数の一致より、あらゆる示強性変数が系のどこでも一致することが簡単に導ける。
石油工学では、相平衡の条件として![]() の一致を挙げる教科書が多いが、これは温度と圧力を既知のパラメータとして暗黙の了解で与えることが多いからである。例えば、セパレーターでのフラッシュを計算するときは温度と圧力が決まっているし(セパレーター条件)、多成分型貯留層シミュレーションで相平衡計算を行うときも温度は固定されており、圧力は流動方程式で与えられるからである。そのような特殊な前提を考えない本来の場合、平衡の条件は次のように書くべきである。
の一致を挙げる教科書が多いが、これは温度と圧力を既知のパラメータとして暗黙の了解で与えることが多いからである。例えば、セパレーターでのフラッシュを計算するときは温度と圧力が決まっているし(セパレーター条件)、多成分型貯留層シミュレーションで相平衡計算を行うときも温度は固定されており、圧力は流動方程式で与えられるからである。そのような特殊な前提を考えない本来の場合、平衡の条件は次のように書くべきである。
(122)